如下图所示,在加热的条件下,一分子炔(alkyne)和一分子双炔(diyne)发生4+2环加成反应,生成活性中间体A。该过程类似于烯烃和双烯环加成的Diels-Alder反应,但反应物比传统D-A反应总共少六个H,所以通常称为Hexadehydro-Diels-Alder反应,简称HDDA。该反应常用于合成多取代芳环。
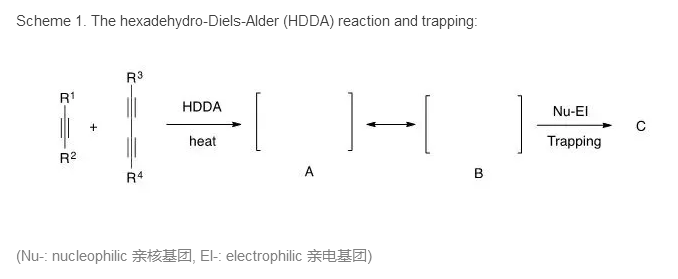
1)画出中间体A的结构和其共振结构B,以及中间体捕获产物C。
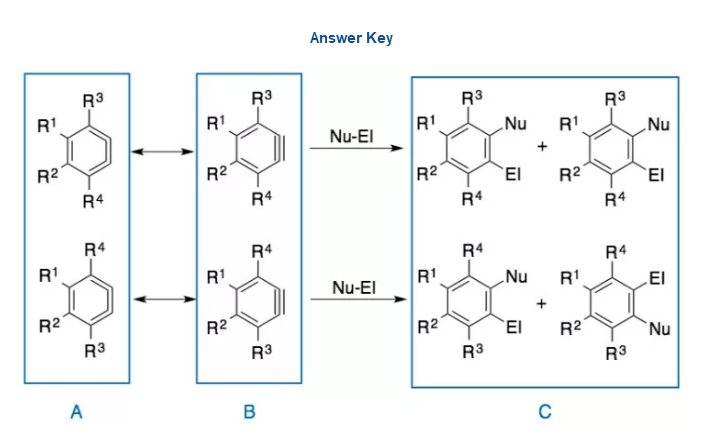
本问是送分题,类比D-A反应(断键和成键),就可以写出A的结构。而后细致一些,注意写全B和C所有的可能结构。
2)HDDA反应常常需要加热才能发生,请简要给出可能的原因,并推测,HDDA是吸热反应还是放热反应?并给出你的理由。
由于生成了新的芳香体系,即使苯炔也有高活性,但HDDA仍然多是强烈放热的反应。但相比于烯和二烯之间的D-A反应,可以想见,构象变化度低的炔和二炔实现前线轨道的靠近、重叠会比较困难,导致活化能较高,所以HDDA反应通常在加热条件下发生。
本题其实考察的是ΔH和Ea的基本概念。
3) 如下图2所示,反应物1通过HDDA过程生成中间体D,而后迅速生成产物E(产率86%)。D和E有相同的分子式。请写出D和E的结构。
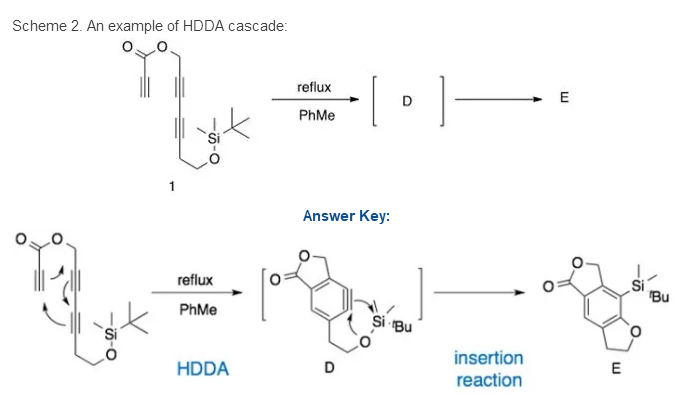
前三问都比较简单,目的是为了让学生了解HDDA反应生成苯炔中间体的机理。为之后的三问做铺垫。
4)但是,如下图Scheme3所示,一个与1结构类似的反应底物2在同样条件下却得到深色的混合物。而若将溶剂由甲苯换为环戊烷(cyclopentane),则生成G和环戊烯。若升高反应物2在环戊烷中的浓度,则G的产率会下降,同时深色混合物亦有生成。请写出G的结构,同时推测深色混合物的可能成分和生成机理。
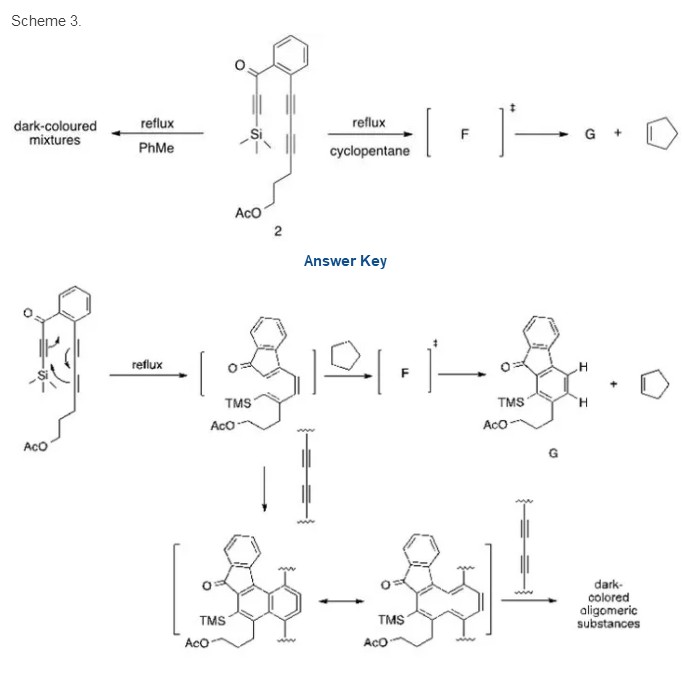
反应底物2经过HDDA过程,苯炔中间体的结构应该很容易写出。然后结合环戊烯的生成,可以推断出G的最可能的结构是苯炔从环戊烷获得了两个H。
本问难点是合理解释深色的混合物副产物是什么。重要的提示是,当反应底物浓度升高时,产率降低,同时副产物增加。因此合理的解释是生成的苯炔与底物双炔继续进行HDDA反应,生成二聚体的芳炔中间体,如此反复,最后得到的是底物2的寡聚体的混合物。另一个可能的产物是苯炔中间体的二聚产物。
5)从烷烃到烯烃的单步反应极为罕见。因此scheme 3中从环戊烷一步生成环戊烯的反应十分吸引人。机理研究发现:反应物2在四氢呋喃(THF)或氘代四氢呋喃(THF-d8)中回流,生成产物G或其二氘代产物G-d2,而未观察到单氘代产物G-d的生成。结果如下表所示。
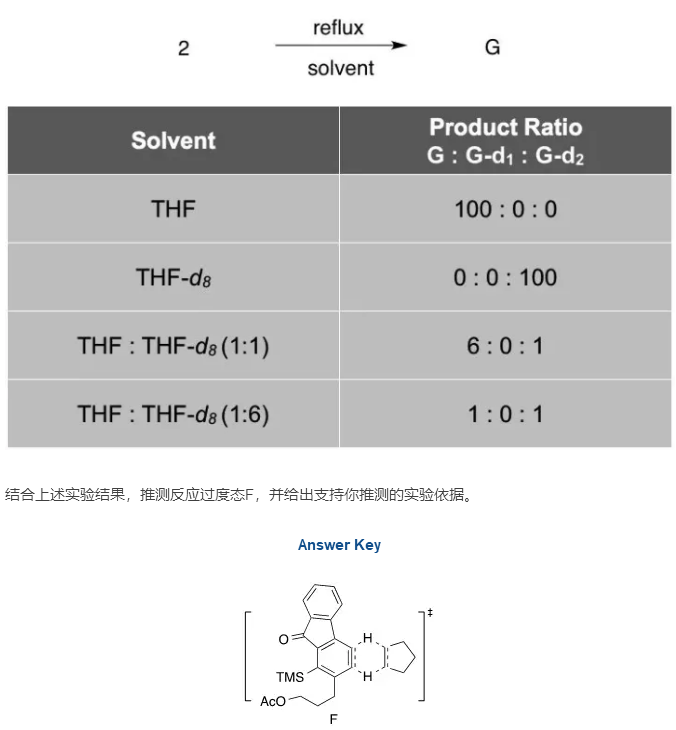
过渡态F的结构不难猜出。比较可能的失分点是将F的结构写成了苯炔中间体。这里需要正确区分中间体和过渡态的区别。中间体是亚稳态,或可以理解为非常活跃的反应物。是可能直接表征甚至分离的。而过渡态是反应路径上的能量峰顶,一般只可间接表征,不能直接观测、分离。
本问的考察重点其实是考生是否能结合实验结果来支撑自己推定的反应机理。这首先需要学生能正确的理解实验目的。
上表罗列了四个氘代实验。
前两个实验证明了从苯炔生成G的质子来源是溶剂分子。
第三个实验用1:1的氘代THF和普通THF的混合溶剂,发现:
1)没有单氘代的G(G-d1)生成;
2)未氘代的G是二氘代的G(G-d2)的六倍。
前者说明捕获一分子苯炔的两个质子均来源于同一分子的溶剂。也就是不存在分步的质子转移机理,亦不存在“苯炔-溶剂-溶剂”的三分子过渡态。
后者则说明该反应存在一级动力学同位素效应(primary KIE, primary kinetic isotope effect),说明通过过渡态F发生质子转移的过程是该反应进程的决速步(RDS, rate-determining step)。
第四个实验目的在于佐证实验三,证明一级KIE效应确实存在,而非来自实验测量误差。
6)在相同的反应物浓度和反应温度的条件下,研究了由不同溶剂分子生成对应烯烃的相对速率(Krel),设定环戊烯的生成速率为1.0。其余烯烃的相对生成速率如下:
环辛烯(2.6),环己烯(0.01),降冰片烯(0.60)。
请依次解释上述三种烯烃相比于环戊烯的生成速率或快或慢的原因。
(降冰片烯的IUPAC命名为:二环[2.2.1]庚-2-烯)。
Answer Key
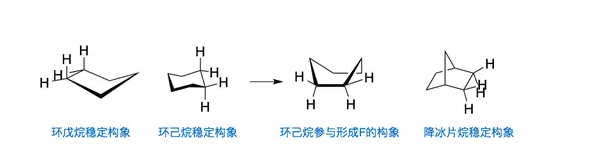
由第5)问已经知道,决速步就是过渡态F的生成。它需要溶剂分子中参与质子转移的H-C-C-H二面角在过渡态F中接近于零。所以这题其实是考环烷烃的构象(conformer)。即考察环烷烃从它的稳定构象过渡到H-C-C-H二面角为零的状态所需要的能量,需要的能量越高,相对速率越慢。
环辛烯(2.6):环辛烷的环张力小于环戊烷,通过旋转C-C键,实现H-C-C-H二面角为零的状态所需能量比较小,所以反应速率比环戊烷快。
环己烯(0.01),降冰片烯(0.60):
环己烷和环戊烷环张力接近。但环己烷的稳定椅式构象需要转化成船式构象才能形成过渡态F,而五元环的稳定构象信封式可以直接参与形成过渡态F。
故而环戊烷的反应速率远大于环己烷。而在二环[2.2.1]庚烷的例子里,六元环受到亚甲基桥的约束,保持在近船式构象,故反应速率远大于环己烷。但由于环被固定,C-C键的转动受限,所以仍然比环戊烷的反应速率慢。
上面就是为大家整理的有机题答案解析的全部内容了,同学们要是还有其他的任何问题和疑问,都欢迎到群:590644810 ,里面有化竞大神为你解答哦!





