为了能帮助同学们更透彻的理解知识点,同时训练化学思维能力,且基于对这个考点难度系数的考虑,我们决定把这道题涉及的知识单独拿出来,并以阅读材料的方式和同学们分享。希望同学们看后能有所收获。
今天阿光老师分享的这道题,主要考察苯炔的结构,即三种互变异构体之间的相互转化。以下是苯炔以双自由基形式存在的三种互变异构体。
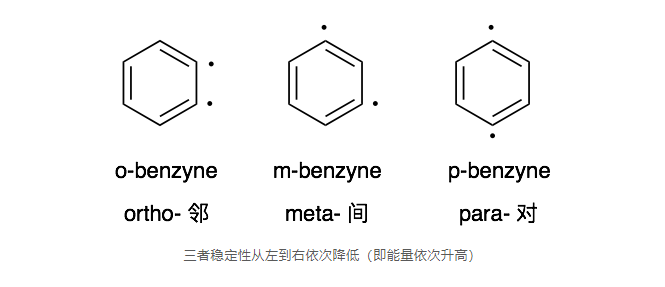
1963年,Fisher和Lossing研究了邻、间、对二碘苯在FVP(Flash Vacuum Pyrolysis, 960°C, 10-3 mbar)条件下的反应中间体。研究的实验结果如下:
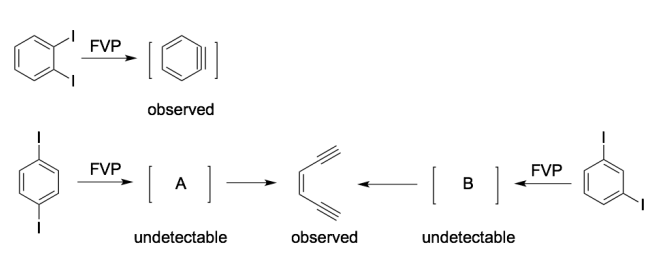
邻二碘苯经过FVP生成了邻苯炔,但间、对二碘苯在真空高温的条件下,都只检测到了烯二炔(enediyne),而没有检测到苯炔中间体。
A和B的结构可以合理的推测为对苯炔(A)和间苯炔(B)。从对苯炔中间体生成烯二炔,是伯格曼环化反应(Bergman Cyclization)的逆过程。但即便不知道Bergman反应,该过程的机理在已知产物的情况下,也相对的显而易见。
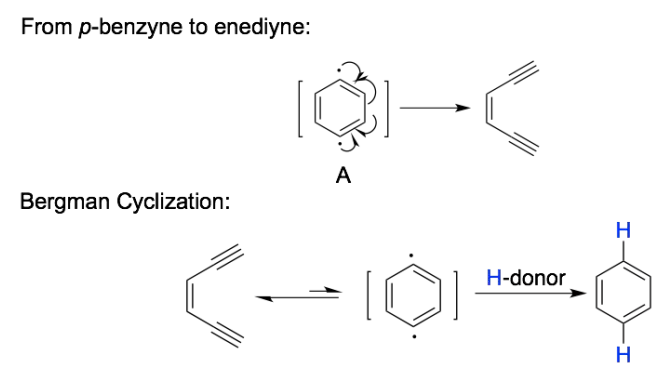
难点是从间苯炔(B)中间体生成烯二炔的反应机理。
首先想到的很可能是间苯炔(B)发生[1,2]-H 迁移,生成对苯炔(A),继而生成烯二炔(如mechanism 1所示)。但计算研究显示,H迁移的能垒非常高,且对苯炔的稳定性差于间苯炔,所以这个过程无论动力学还是热力学上都是不利的。
从另一角度看,如果可以越过能垒发生[1,2]-H迁移,间苯炔会更倾向于生成相对稳定的邻苯炔。故,mechanism 1不是合理的机理。
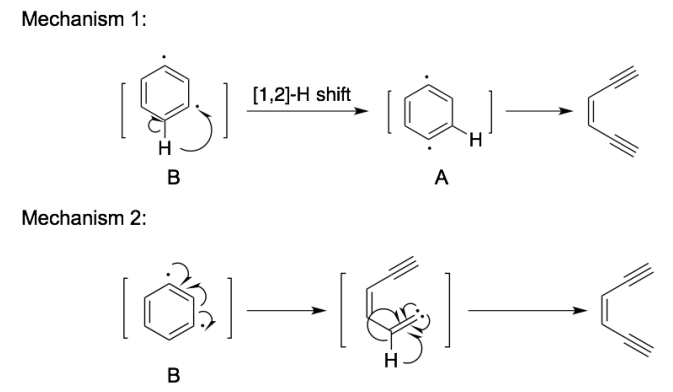
计算化学的研究显示(如mechanism 2所示),最可能的反应路径是间苯炔发生开环,生成一个亚烷基卡宾中间体,随后迅速的重排,生成烯二炔。
苯炔结构转化机理难就难在这里“合理”的反应路径经过了苯环的开环,而这种失去芳香性的中间体,在绝大多数的机理推测中,都是不优先考虑的,是违背“常识”的。
这里可以发生的原因是间苯炔、对苯炔的高度不稳定性,以及苛刻的反应条件,如非常高的温度。
邻苯炔中间体较间、对苯炔稳定,在写机理的时候不优先考虑开环。但如果伴随合适的捕捉、或重拍过程,生成更稳定的产物,即后续的反应能提供足够的驱动力,也是有可能出现开环的机理的。
下图就是一个例子,不过如果考察这样的机理,一般题干会给予足够的提示和引导,所以不需要死记硬背。
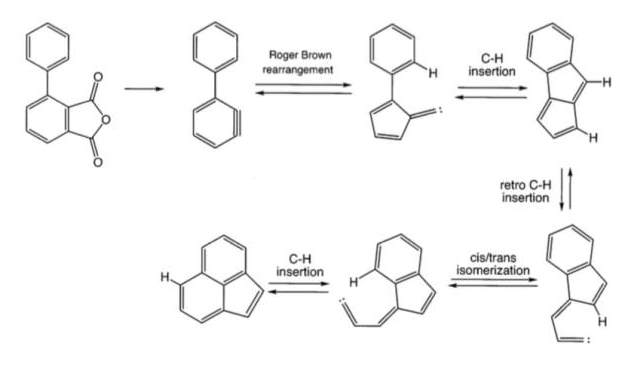
这就要求学生:
1)对有机化学的基本概念有透彻的理解。
2)能理解常见反应的反应机理。
满足这两条,学生就具备了有机化学的“常识”,在画反应机理的时候就能对“合理性”有基本正确的判断。
另外,我们的化学竞赛网站刚刚起步,有任何关于化学竞赛的疑问,或者你想要看关于化学竞赛哪方面的资料,可以进入我们的QQ群:590644810,里面有化竞金牌为你答疑哦!





